中国药神诞生记
- 来源:21世纪商业评论
- 关键字:商业化,产品,新势力
- 发布时间:2019-05-05 21:43

2019年2月26日,一个普通的周二,因为一张处方,成为中国医药史上特别的一天,尤其对于中国黑色素瘤患者来说,这一天可能是生与死的分界。
当天下午4时,第一批“特瑞普利”单抗注射液(商品名:拓益)运抵北京大学肿瘤医院药房,首个国产抗癌药PD-1单抗产品正式到货,启动全国销售。
为这一天,拓益走了三年多的旅程:2015年12月,获得国内首个PD-1单抗临床批件;2018年3月,又成为首个被受理新药注册的国产PD-1;次月,药品注册申请进入优先评审程序;同年12月,产品获批上市,获批的适应证是既往接受全身系统治疗失败的不可切除或转移性黑色素瘤,较之以往,这个速度至少节约了一半时间。
黑色素瘤有“癌中之王”之称,很多人听说它是因电影《非诚勿扰2》,致病凶险,死亡率又高,是进展最快、预后最不好也最为难治的恶性肿瘤之一,治疗耗费甚巨。
出品方君实生物为拓益的定价为7200元/240mg(支),合30元/mg,年治疗费用187200元的价格,同样适应证的进口产品“帕博利珠”单抗价格为17918元/100mg(支),合179元/mg,年治疗费用609212元,前者仅为后者1/3(对比以平均体重60kg计算),为目前同类药的全球最低价。
若符合北京白求恩公益基金会的赠药计划,使用4个周期后可获4个周期的药品援助,那么,患者一年用药负担约为93600元。对于常年支付着高昂的进口治疗费用,或者需以各种灰色手段境外购药的患者,拓益问世无异于“药神”降临。
拓益的获批开了个好头,其后国产治癌新药喜讯连连。
2018年12月,信达生物的PD-1抗体药物“信迪利单抗注射液”在国内获批上市,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗;2019年1月,百濟神州一款在研的布鲁顿氏酪氨酸激酶(BTK)抑制剂Zanubrutinib,获得美国FDA突破性疗法认定,用于治疗先前至少接受过一种治疗的成年套细胞淋巴瘤(MCL)患者;同年2月,复宏汉霖(复星医药旗下)研制的国内首个生物类似药也宣布获批,主要用于非霍奇金淋巴瘤的治疗。
好事频传,国药高光之下,医药市场正在形成新的利益格局,“中国药神”正在崛起。
救命处方
终于能卖国产PD-1了。兴奋的不只是患者,还有医护人员。
拓益的第一张处方比预计早了一天,医药同行与媒体们本来翘首以盼,等着见证2019年2月27日一早处方开具的时刻,但是,北京大学肿瘤医院副院长、中国临床肿瘤学会(CSCO)秘书长郭军没忍住。郭军是中国黑色素瘤研究领域领军人物,业内有个霸气的称呼叫“黑老大”,也是拓益注册临床研究的牵头人。
2月26日,郭军已离开办公室准备走出医院,一听说药品运抵药房,便折回诊室,开出了首张拓益处方。第一位受益者张瑶(化名),原本只能寄希望于价格高昂的进口药,现在有了新的选择。
对于黑色素瘤患者来说,每一种有可能的治疗,都是一根救命稻草。
1972年,达卡巴嗪(Dacarbazine)获FDA批准用于黑色素瘤的化疗,此后数十年,只有早期黑色素瘤可以局部手术治疗,其他患者则以化疗为主。然而,数据显示,黑色素瘤化疗的有效率仅为10%-20%,甚至有些只有6%-7%,即便是有效,也仅能控制肿瘤1.7个月,无法提高总生存时间。
12年前,PD-1抑制剂正式进行人体试验。美国约翰霍普金斯大学肿瘤免疫治疗泰斗陈列平教授,参与组织了全球首个PD-1抑制剂针对肿瘤患者的临床试验,证明PD-1抑制剂针对恶性黑色素瘤、肾癌和肺癌有效,黑色素瘤的治疗才迎来了新的曙光。
君实生物CEO李宁向《21CBR》记者解释,传统的化疗和靶向治疗,狙击的是肿瘤细胞本身,“我们将化疗称为细胞毒治疗,以毒杀癌细胞来达到杀死肿瘤的目的,而PD-1的治疗路径完全不同”。PD-1抗体作用于人的免疫系统,通过激活被肿瘤细胞抑制的T淋巴细胞,使免疫系统正常化。
“这样能使人体免疫与肿瘤达到一种平衡,有些通过联合用药,甚至能彻底消除肿瘤。”李宁说,从治疗领域来说,目前尚未有一款抗肿瘤药能如PD-1这样广谱,几乎所有系统的肿瘤都被证实有一定效果,“以往化疗只针对一到两个器官,PD-1几乎全身有效,且在有效性和安全性都成效明显。”
值得一提的是,2018年诺贝尔生理学/医学奖授予美国免疫学家詹姆斯.艾利森(James Allison)与日本生物学家本庶佑(Tasuku Honjo),即表彰其“发现负性免疫调节治疗癌症的疗法”的贡献,即以自身免疫系统抗击癌症的疗法。
在诺贝尔奖项授予该奖项前,这个前沿科技就已得到了市场的验证。2014年7月,日本批准首个PD-1抗体百时美施贵宝欧狄沃Opdivo(俗称O药)上市,针对恶性黑色素瘤;2个月后,PD-1抗体帕博利珠单抗Keytruda(俗称K药)在美批准上市。随后,针对非小细胞肺癌、肾癌等适应症的PD-1抑制剂陆续在美国、欧洲获批。2018年8月,O药在中国上市首日,销售额就突破5000万元。
根据君实生物提供的数据,过去接受过不可切除或转移性黑色素瘤全身系统治疗失败的患者,经过拓益单药治疗后,约 17.3% 病患的肿瘤缩小到一定量并能维持一定时间,疾病控制率(DCR)为57.5%、1年生存率为69.3%。且无论患者经历过几线治疗,或者黑色素瘤为何种亚型,拓益的疾病控制率都很稳定。其中,就国人高发的黏膜黑色素瘤,拓益与血管生成抑制剂的联合治疗项目,早期临床数据有效率超过60%。
这些苍白的数字背后,是一个个生命活下来的希望。
李宁表示,在临床数据上,相比进口药,国产PD-1的疗效至少已经追平。“从生存的角度来说,经拓益治疗后的黑色素瘤患者,其中位总生存期约为24个月,用K药的中位生存时间不到13个月。从疾病控制率的角度,60%的病人得到了控制,用药后肿瘤不长或者缩小。”根据K药的说明书,K药的中位总生存期为12.1个月,疾病控制率为38.2%。
这样的数据,激励君实生物进入几乎所有中国高发恶性肿瘤的临床研究,除了现有的适应证外,针对鼻咽癌、胃癌、食管癌、尿路上皮癌、肺癌等10多个瘤种的试验也同时开发,而平均一个瘤种三期临床试验成本总和约为2亿-3亿元。从早期临床数据来看,国产PD-1均有成效,有机会成为广谱抗癌药物。
君实生物加足马力全线铺开,无疑是想尽快打开市场,对于国内一批创新药企而言,窗口期才刚到来。
新势力拐点
2009年,中国迎来第二次医疗改革,IPO市场重新开闸,那年6月,陈海刚从北京协和医院毕业,加入投资银行,成为一名医药行业分析师。过去10年,其服务了中国第一代医药公司或者IPO项目,见证它们收入与利润的快速成长。
“分析中国医药企业的产品线,过去是化学仿制药的天下,缺乏生物技术公司,没有IP与原创知识产权。”陈海刚说,过去三四十年,中国医药消费市场急速膨胀,形成营商红利,一批人依靠强大的销售能力,就可以赚到第一桶金;反观自主研发创新药,动辄耗时10年、耗费10亿美元的单一新药研发,未必能上市获得商业回报,显然很不划算,拥有超过7000家医药公司的中国,研发一直大而不强。
“即便做药,很多产品与科学的关联性不强,企业家也并非医药背景,第一代医药企业多以销售为主导。”陈海刚告诉《21CBR》记者。

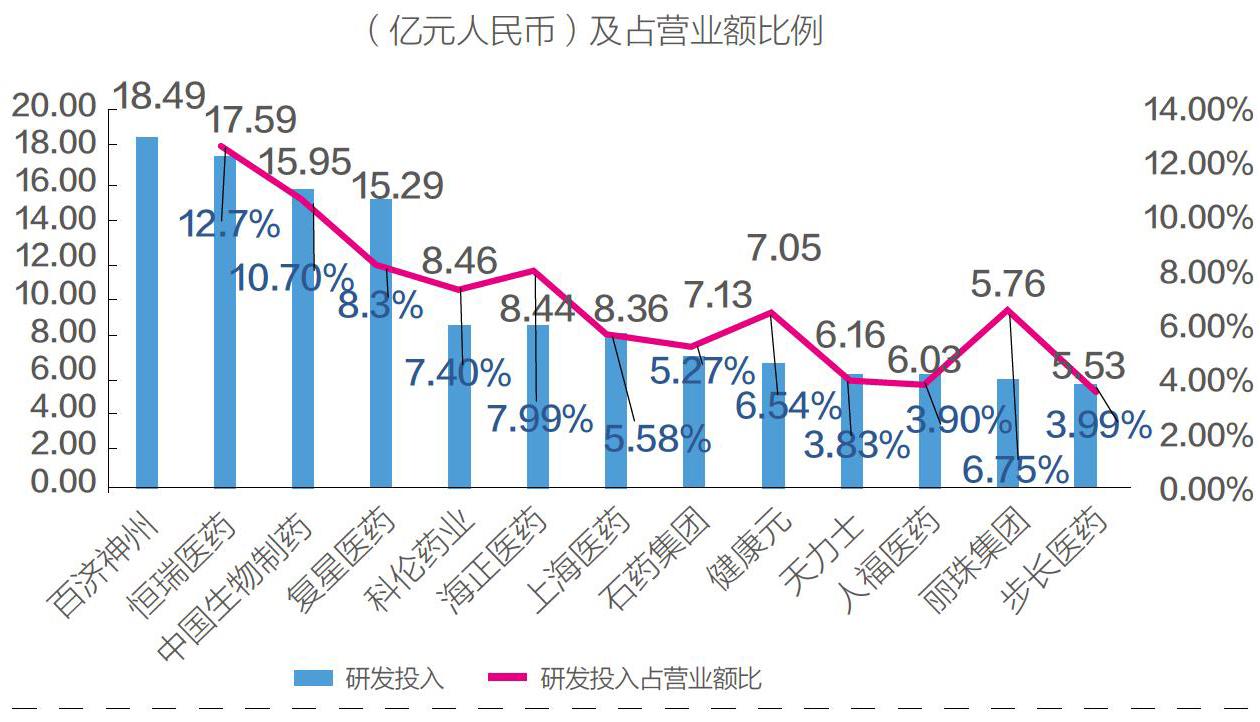
2017 年中国A 股和港股研发投入大于5 亿元公司研发投入额

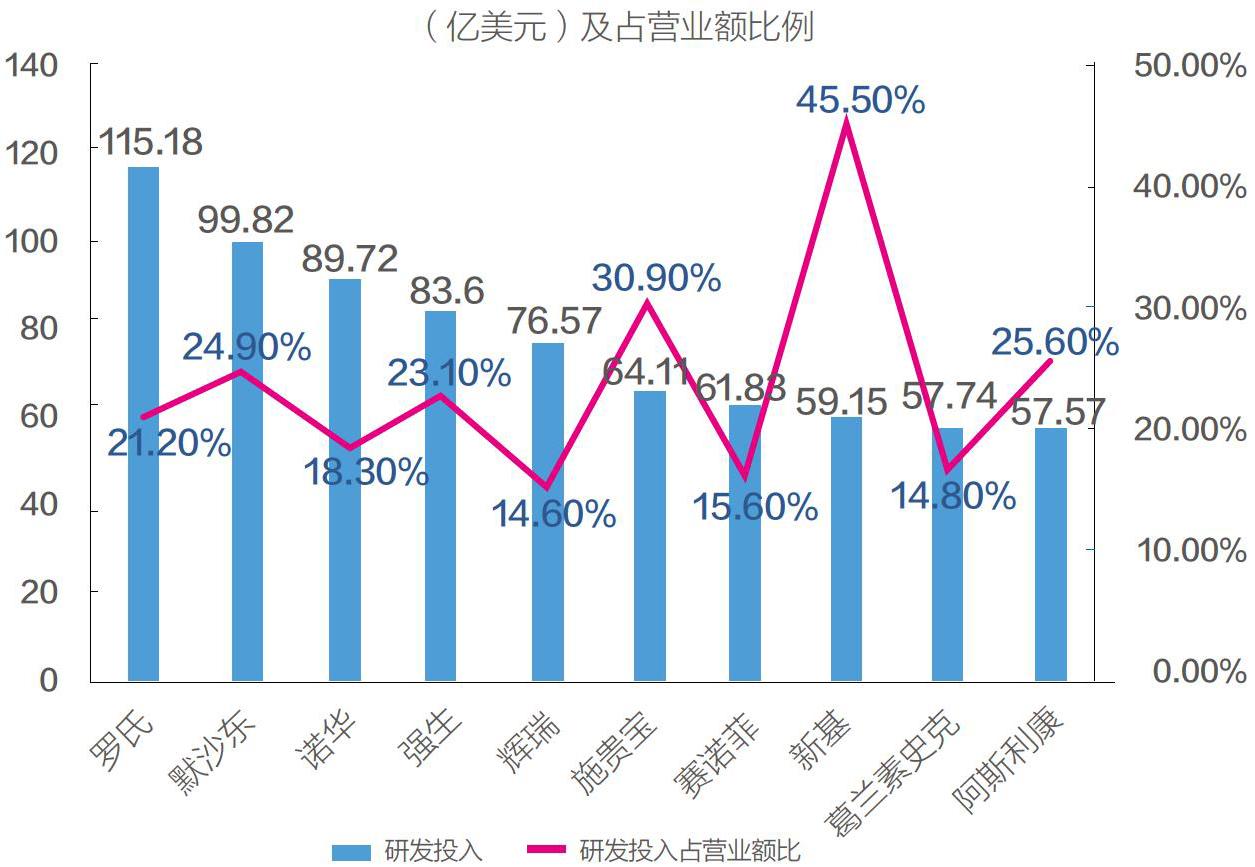
2017 年度全球药企研发投入10 强企业研发投入额数据来源:wind,华夏基石
2015年,陈海刚离开二级市场,加入杏泽资本,从事医疗健康投资,职业生涯有了新起点,这一年,中国医药行业迎来分水岭。
“2015年前后,中国有了第一批生物技术公司,抗体、CART等初创企业开始大量涌现,相比第一代,这批创新药企有了明显的迭代,形成了代际差。”陈海刚明显感受到,很多研发驱动型的公司冒了出来,产品有明确作用机理,在临床有真正价值,且创始团队大多是科学家出身。
浪成于微澜之间,这股医药新势力崛起,有多重力量的助推。
首先,是人的因素。
生物制药领域是精英创业,并非有良好市場感觉、理解消费者需求就能成功的,往往需很长时间的科学训练。
按成立时间细数国内创新药企的创始人,清一色华丽的履历:百济神州创始人、科学顾问委员会主席王晓东,为美国国家科学院院士、中国科学院外籍院士以及北京生命科学研究所所长;信达生物制药创始人俞德超,中国科学院分子遗传学博士,美国加州大学博士后,全球肿瘤病毒疗法的主要创始人之一;歌礼制药创始人吴劲梓,创业之前在美国担任葛兰素史克HIV药物发现执行部门副总裁;再鼎医药创始人杜莹,曾是和记黄埔医药创建人……
其中,很多人是上世纪80年代第一批留学生,经过海外的学习和工作,阅历、知识、能力到位,已具备创业的资本和底气。2017年后,又有一波外企资深高管回流本土创新企业。
2017年3月,王立群加入复星凯特,成为公司CEO,此前在百时美施贵宝、阿斯利康以及葛兰素史克中国研发中心任职多年;2018年1月,李宁从赛诺菲副总裁的岗位上离职,加入君实生物;4个月后,辉瑞中国国家经理兼辉瑞核心医疗大中华区总裁吴晓滨宣布离职,随后百济神州官宣其成为中国区总经理兼总裁;同一时间段,再鼎医药公告原阿斯利康中国副总裁、肿瘤业务负责人梁怡加入,成为首席商务官、大中华区总裁。
吴晓滨回忆,2014年第一次接触百济神州,觉得这家公司了不起,因为当时感觉在中国做创新药“是件挺遥远的事”,直到公司有人离职去了百济神州,他才重新看待这件事;2017年前后,陆续有六七家本土创新药企向梁怡抛出绣球,他选择了再鼎,第一次听到其名字是2015年负责阿斯利康肿瘤业务时,“当时很巧,再鼎引进的产品管线我也在关注,才了解到这家本土公司”。
同时,专业投资人也开始出现了。
陈海刚坦言,医药投资,出资只是一方面,更重要是做对的判断,如果一开始立项在药物靶标上选择错误,再多的钱都是徒劳,“互联网有流量或者运营数据指标,对生物技术公司而言,资本要理解公司所做的事情,所选择的靶标与相应的作用机理,这都需要时间”。

在美国,苹果公司与基因泰克(全球第一家生物技术公司)同在1976年创立, IT与生物技术两个方向的创投几乎同时起步。在中国,生物技术领域的VC晚了十来年,近些年也开始活跃起来。
另外,制度环境发生了剧烈变化。用中国医药创新促进会(PhIRDA)执行会长宋瑞霖的话说,看待中国生物医药产业,要回溯到2015年。
这一年,CFDA〔国家食品药品监督管理总局,现已重新组建NMPA(国家药品监督管理局)〕启动一系列中国医药政策改革方案,最核心的两个举措:一是开展临床自查,启动仿制药一致性评价工作,对已经批准上市的仿制药,按与原研药品质量和疗效一致的原则,分期分批进行质量一致性评价,仿制药需在质量与药效上达到与原研药一致的水平;二是提高新药审批各环节的效率,海外多中心临床包含足够多的中国数据,即可直接申报。
这种主动求变,有着深刻的现实压力,中国人口老龄化加剧,疾病尤其恶性肿瘤发病率与绝对数连年攀升,民众的健康投入也不断提升,这要求药物审评审批制度与时俱进。
旧有《药品注册管理办法》下,对于仿制药生物等效性试验的标准不清,申报与审批过程中存在不少漏洞。有业内人士为《21CBR》记者打了个比方:“仿制药在药效上应对标原研药,国内以往的标准,却允许仿制药对标市面上的仿制药。直白地说,对标100分的原研药,仿制药能做到80分,对标只有80分的仿制药,再生产出的药品就不是一回事了。”
原研药都有一个专利保护期,本来专利期过后,仿制药上市,该药品价格自动降低,既鼓励原研药企不断推陈出新,又提高了医疗可及性。可由于国内仿制药质量不过关,专利保护在中国失效,原研药始终能以高价垄断市场,创新动力不足,医疗成本高企。
一边是仿制药质量跟不上,一边则是新药上市审批滞后。原本按照CFDA规定,进入中国市场的创新药品,需提交在中国人身上的试验数据,本意是确保有效性和安全性,可临床试验往往要有1-3年完成,加上评审积压的时间,以往创新药品国内上市往往比国外滯后5年以上,自主研发药物时间更要耗时10年以上。
回国前,李宁曾历任美国FDA审评员、高级审评员、审评组长、分部主任等职务。他发现,中国新药审批速度慢,也受制于审评人员匮乏。“美国3亿人口,审评人员数千,我们14亿人口,技术审评人员只有100多个人,以至批准一个临床研究,就要等两年时间。”
新政落地就像是一种刀锋上的利益纠错,旨在让仿制药角色回归,原研药专利到期价格下降,新药上市加速,全社会医疗成本能够降低,按照时任国家食品药品监督管理总局副局长吴浈当年的说法,“只要临床需要,公众有用,来得越早,对公众越有益”。2017年,CFDA正式加入国际人用药品注册技术协调会(ICH),药品审批逐步与国际接轨,差距明显缩小,现在通常一个临床审批,3个月就可以完成。
2008-2018年,中国一共批了38个1类创新药,2018年就批了9个,占了近四分之一,这一年,中国批准罗沙司他(roxadustat,商品名为爱瑞卓)上市,这是由珐博进(FibroGen)和阿斯利康带来的一款“first-in-class”新药,治疗肾性贫血,目前尚未在其他任何国家上市。这是中国第一次超越国外,在全球首次上市新药。
九死一生
新药研发,先驱和先烈往往只在一线间。
2012年4月,重庆啤酒公告,其疫苗二期临床试验无效,此后11个交易日,走出10个跌停板。此前,从上市收购佳辰生物开始,乙肝疫苗的进展就推动着其股价扶摇直上,撇开概念炒作因素,股价重挫说明了创新失败后的惨烈。
一家副业做医药的公司尚且如此,一门心思研发新品的药企,更是九死一生。业内盛传,一家已上市的创新药企,2013年底账上仅剩数万元,连接上门的数拨投资人都无投资意向,一批创始员工熬不下去,选择离职,只是念及同甘苦的情谊,公司保留了他们持有的原始股份,没料想,数年后公司IPO,这一批人意外身价翻番。
新药研究,不只要有技术,还必须有商业模式。
再鼎医药于2014年成立,定位研发癌症、自身免疫和感染性疾病的创新型生物制药公司,在创立伊始,就建立自主研发和外部引进“双轮驱动”的模式,随后又在苏州建立两座生产工厂,未来上市药物将实现本土生产,并建立全国性的商业化团队。
梁怡坦承,即便再鼎2015年开始研发新药,以10-15年的周期计算,2030年才可能看到成果,而现在的研发合作模式,是站在巨人肩膀上加速前进,“我们并不是简单地License-in,将产品引进在中国销售,而是共同完成在中国的开发并实现商业化。”
2018年12月,再鼎首个商业化产品——则乐(Niraparib)即告上市,这是中国香港首个获批用于所有铂敏感复发卵巢癌患者维持治疗(无论 BRCA 是否突变)的 PARP 抑制剂,此前该产品已在美国和欧洲获批。迈出商业化第一步,研发、创新就有了正向现金流作支撑。
PD-1上市的前前后后,临床费用耗资约15亿元人民币,李宁感叹,一直面临不确定带来的焦虑,“临床申请能不能批,临床研究失败了怎么办?产品上市递交能否成功?每个不同时间点都在做关乎企业生死存亡的决策。”此前,李宁在跨国企业管辖过20多个国家的业务,即便有挑战,也与现在的生死时速截然不同。
“公司创立时,考虑过高风险、高投入的代价,也曾计划做生物仿制药,譬如靶向药,当时国家的政策也鼓励,产品稳,至少生存不会有问题。要做新药,很多连临床研究怎么做都没谱。”李宁回忆,加入君实生物开始,整个团队铆足劲,一心只想要让产品上市,回想也后怕,万一出现差池,团队这么多人要怎么办?
好在顶层设计为医药研发推了一把力。2018年,国家医保局决定启动“4+7”城市带量采购的试点,通过明确采购量,低价者中标的方式完成药品采购,这一次可谓从支付端倒逼创新。
简单说,即在通过一致性评价的仿制药对应的通用名品种中进行定价、定量招标,试点的11座城市拿出60%~70%的市场份额给中标企业,中标者以量换价,其他只能分享剩余 30%~40%的份额。短期看,药企销售利润势必会受影响,长期看,仿制药企估值将迅速遇到天花板,因为一旦某品种通过一致性评价的企业达到3家以上,价格竞争剧烈,仿制药企只能靠多品种、低成本存活。
政策落地,很快传导至资本市场。2018年9月,新政座谈会一结束,A股、港股市场的医药股就一路杀跌,尤其港股市场,14只医药股一天蒸发数百亿元。
2019年1月3日,中国生物制药(01177.HK)市值跌至583.69亿港币,而百济神州(06160.HK),当天市值为625.08亿港币。一家年利润21亿港币的药企,居然与一家持续亏损的同行出现市值倒挂。有人将这一天,看作是中国医药创新时代的分界线,医药巨头开始重新排位。
巨大的前景下,人才在加速聚集,资本也更踊跃,愿意承担高风险。
2018年加入百济神州后,吴晓滨发现,公司内部科学家们对新靶点、科研文章、治疗方法的优点缺点等如数家珍。临床试验水平,不光速度快、效率高,且是在全球多中心开展,“在很多方面变成我需要去学习的了”。
“在君实生物,‘第一这个词听得太多了:第一个获得PD-1临床批件、第一个PD-1被批上市……但另一面是缺经验。”李宁坦言,从公司层面看,每一步都是从0到1,不过,团队大部分成员均来自国内或者国际创新药企,经历过很多“第一”的肿瘤药诞生,个人经验可以填补公司经验的空白。例如,药品注册需用国际格式递交,全中国做过的人可能都寥寥无几,但公司很多来自外企的员工,包括在FDA工作多年的李宁却熟悉,知道如何表述临床研究数据来帮助药监部门更好地理解,这样能少走不少弯路。
梁怡加入再鼎后,首先就建立起了内地、香港和澳门的商业化团队,尤其在香港,团队筹建速度惊人,2个月里组建起20人的商业化团队。此前这家公司只有研发部门,销售团队的到位推动了产品的上市,其管理体系与成熟的跨国企业一脉相承,“‘4+7试点后,最大的感受是招人容易了,大家开始感受到,在不远的将来,本土创新药企将崛起成为行业的一股新势力”。
资本也增势迅猛。根据动脉网数据库的统计,2017年,全球医疗健康领域融资规模达1571亿元人民币,同比增57%。2017年年底,港股上市制度作出重大调整,“允许无收入生物科技企业在香港上市,预期最低市值须达15亿港元”,为新药研发企业的公开募集开了口子。
陈海刚明显感受到了市场的升温,由于恰好碰上行业的快速上升期,所持有项目的估值,相比四年前有明显上涨,基金账面回报水涨船高。
中国1.1 类新药临床申请情况数据来源:药渡,华夏基石
他甚至因为高估值放弃部分項目,“研发要符合客观规律,资本现在给到一个很高的估值,下次多长时间做出一个什么样的临床结果,这个很难人为改变的,容易透支未来……2018年下半年由于项目估值原因,我们放慢了投资的速率,错过了一些项目”。
直道聚焦
相比PD-1,CAR-T疗法显得命运多舛。
2016年“魏则西事件”爆发,其中,被证明无效的CIK疗法,令细胞免疫治疗备受怀疑,也使得临床疗效不俗的CAR-T技术蒙冤,其后,Juno旗下CAR-T产品 JCAR015又遭放弃。幸而2017年,FDA批准两款CAR-T产品,分别是诺华的Kymriah和Kite/Gilead的Yescarta,才为新疗法正名。
3月初接受《21CBR》记者采访前,王立群正与管理团队讨论“两会”,他希望能有代表为细胞治疗的监管政策建言。
就在2月末,国家卫生健康委员会起草了《生物医学新技术临床应用管理条例(征求意见稿)》,后在官网刊发了《关于政协十三届全国委员会第一次会议第4443号(医疗体育类434号)提案答复的函》,其中谈及,体细胞治疗肿瘤等难治性疾病展现出良好的应用前景,“卫建委将全力支持细胞治疗产品申报药物注册,组织开展细胞治疗技术临床研究机构申报、遴选、备案”。

复星凯特正加速CAR-T商业化进程,在王立群看来,卫健委推出管理办法的目的在于,规范生物医学新技术的临床研究,保障医疗质量安全,加速领先科技的临床转化应用,可征求意见稿中未对“生物医学新技术”进行明确界定和区分,尤其未对体细胞技术进行分类管理。
他解释说,细胞治疗有高危和低危之别,CAR-T细胞治疗作为高危产品,必须按药品进行申报和监管,如对细胞治疗产品以双轨制进行监管,可能导致行业质量标准以及临床研究规范的混淆,影响行业规范化发展。对于患者而言,只有在严格监管下的CAR-T产品,才能保障其安全和利益。
“此前CAR-T企业已形成共识,有几十个IND申报且有十几个经过CDE(国家食品药品监督管理局药品审评中心)审评而获批临床试验。CDE采用宽进严出的逻辑,以开放的态度允许更多细胞治疗产品,通过严谨的临床试验来验证能否拥有上市许可。”王立群认为,双轨制存在会让人担心,如果卫健委的标准比药审中心低,会动摇以高投资、高质量开发细胞治疗产品企业的决心,CDE刚形成的药监管理就形同虚设,好的细胞治疗便不能像其他药物一样广泛应用于临床,造福患者,与ICH(国际人用药品注册技术协调会)要求和国际接轨相偏离。
另一位CAR-T从业人员表达了同样的担忧:“按照现在的准入机制,不少CAR-T产品在两三年内就有可能上市,着急放口子,弊大于利。”
韩璐
相比王立群的准入担忧,李宁密切关注着合理用药问题。
进口药贵、疗效好,是中国患者的普遍认知。要完成国产替代,价格便宜不够,更要树立疗效威望,临床用药的有效率是硬指标。真正做到对症下药,就包括医生能否识别出满足使用条件的患者?真正能够获益的患者能否正确使用药物?
目前,君实生物的销售团队大概140人左右,李宁要求很简单,就是去教育医生,让他们了解药物风险、效果以及适用的患者条件,“我希望使用拓益的患者都能够100%获益,严格的筛选方式会在短期内影响销售额,实际上建立了长期的品牌效应”。
李宁告诉《21CBR》记者,在君实生物的销售部门,KPI考核重心是比疗效,“我们会追踪进行学术推广的医院,以及医生为病人开出处方以后的有效率,同一种药,如果A销售有效率达到50%,B销售只有20%,就是对症与否的差别了”。
李寧向《21CBR》记者展示了内部使用的培训资料 “蓝宝书”和“红宝书”,专门介绍肿瘤免疫治疗的基本原理、不同药物的治疗方法、临床表现等,“肿瘤免疫药是一个新鲜事物,与以前的有着十几年使用过程的靶向药和化疗药不一样,用药时间短,即使在国外用药经验也很缺乏,行业有责任对医生、病人进行教育,第一它不是神药,第二要正确使用,前景很广,要走的路很长”。对于商业化的进程,李宁表现得非常谨慎。
王立群和李宁的担忧,揭示了新药研发系统性的挑战,“弯道超车”一词在中国各行业非常流行,偏偏在问到创新药企能否实现时,几乎所有人的回答都是——“未来可期,但要奋起直追。”
李宁认为,在生物医药的基础研究方面,欧美药企更为领先,“毕竟土壤要肥沃很多,生长、开花、结果相对要容易,我们在创新的基础层面确实有些欠缺。”
资源投入也不可同日而语。2017年,A股医药生物类共275家上市公司,研发投入总和320亿元人民币,其中81家药企研发投入过亿元,恒瑞医药以17.59亿元位居首位,复星医药15.29亿元位居第二;同年,跨国药企前十强金额均超过50亿美元,罗氏一家的支出就高达115亿美元。对比外国同行的一掷千金,国内公司相形见绌。
此外,很多基础研究和标准建立,中国还在补课之中。“我们技术审评能力以及审评人员素质提升很快,但是也不能不看到差距。”李宁以PD-1举例,拓益在中国批准上市只比K药、O药晚3-6个月,看上去不是很长,其实后两者的临床研究做了非常多,中国才刚刚开始,“其中就有重复研究的问题,如果某一项资料已经变成标准资料,后来者就没有做临床研究的必要性,这种数据标准目前还是空白”。
梁怡认为,中国医药行业的发展轨迹,可能是“没有时间表的三步走”:第一步,做好仿制药;第二步,在仿制药基础上做创新;第三步,以创新药占主导;其间,比拼的是耐心和专注,比的是守住对的事,且能坚持做下去,能力与组织结构的匹配决定了发展速度,“现在正是小江小河汇成河流的时候,应该集中朝着一个趋势去,千万不要在这个过程中,随意停留、转向,这条路走得越直,目标越清晰越好”。
“永远要保持学习的心态,各方面能力齐备后,自然而然很多创新才会爆发。”梁怡直言,商业浪潮之下,诱惑不少,比如开发市场前景良好的普药产品,“我们的原则就是做创新特药,这是立身之本也是筛选产品的标准。”
君实生物即将享受坚守带来的红利。
“PD-1的市场规模足够大,可以容纳足够多的产品。如果产品有自己的特性,有合适的治疗和联合治疗,那么相对过千万的新发、存量病人,会有很大的空间。”李宁认为,一旦更多国产PD-1上市,有更好的性价比,将可能在癌症治疗领域与进口药形成7:3甚至8:2的格局,“国产药品占据主导完全有可能,前提是确保安全性和有效性”。
吴晓滨说,药物研发整体上风险蛮大,“中国目前研发形势大好,好像还没听过失败或者很少有失败的例子,随着我们国家新药研发的不断推进,早晚有一天会面临这样的情况,那时候,我们企业家、投资人又是否做好了心理准备?”
 关注读览天下微信,
100万篇深度好文,
等你来看……
关注读览天下微信,
100万篇深度好文,
等你来看……